Die 12 Hallmarks of Aging
Altern ist kein einzelner Vorgang, sondern das Zusammenspiel mehrerer biologischer Prozesse, die sich über Jahrzehnte entwickeln. Die moderne Altersforschung hat diese Prozesse systematisch beschrieben und zu den sogenannten Hallmarks of Aging zusammengefasst. Sie erklären, warum sich Zellen verändern, Gewebe an Stabilität verlieren und die Regeneration langsamer wird.
In der aktualisierten Fassung von 2023 umfasst dieses Modell 12 zentrale Kennzeichen, die gemeinsam bestimmen, wie schnell oder langsam der Körper altert. Sie bilden heute die wissenschaftliche Grundlage vieler Longevity-Ansätze.
1. Genomische Instabilität
Im Laufe des Lebens ist unsere DNA ständig Belastungen ausgesetzt, etwa durch Stoffwechselprozesse, Umweltfaktoren oder oxidativen Stress. Zwar verfügt der Körper über Reparaturmechanismen, doch deren Effizienz nimmt mit dem Alter ab. Unreparierte DNA-Schäden können dazu führen, dass Zellen fehlerhaft arbeiten oder ihre Funktion verlieren. Diese Instabilität gilt als eine der grundlegenden Ursachen biologischen Alterns.

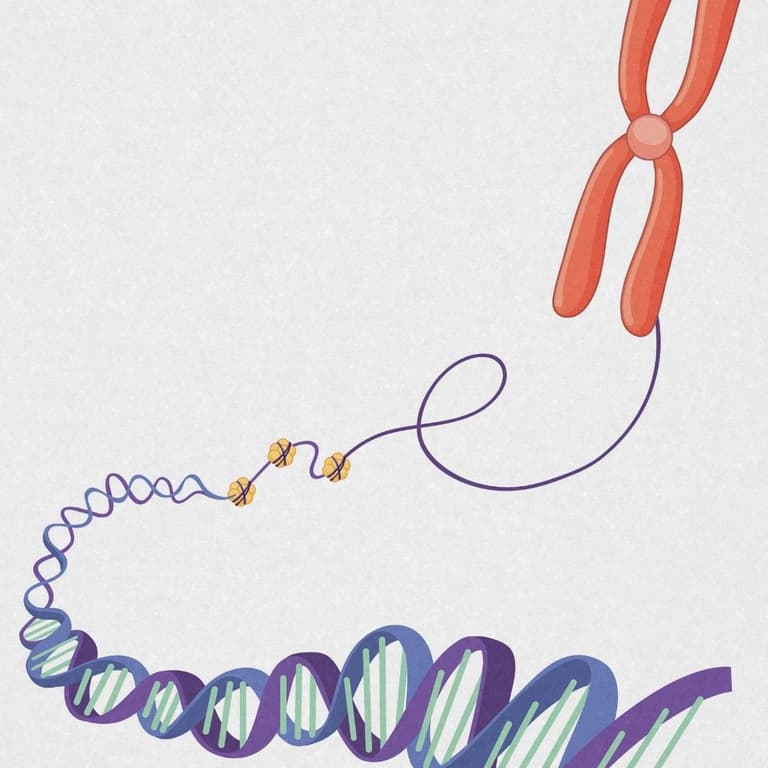
2. Telomerverkürzung
Telomere schützen die Enden unserer Chromosomen und verkürzen sich mit jeder Zellteilung. Wird eine kritische Länge unterschritten, verliert die Zelle ihre Teilungsfähigkeit oder geht in einen Ruhestand über. Dieser Prozess begrenzt die Regenerationsfähigkeit von Geweben. Telomerverkürzung steht daher in engem Zusammenhang mit Zellalterung und Funktionsverlust.
3. Epigenetische Veränderungen
Epigenetische Mechanismen steuern, welche Gene aktiv oder inaktiv sind. Mit zunehmendem Alter kommt es zu Verschiebungen dieser Steuerung, wodurch Gene falsch reguliert werden. Das kann Entzündungsprozesse verstärken oder Reparaturmechanismen abschwächen. Obwohl die DNA selbst unverändert bleibt, verändert sich so ihre funktionelle Nutzung.
4. Verlust der Proteostase
Zellen müssen Proteine korrekt falten, reparieren und abbauen. Mit dem Alter funktioniert dieses Gleichgewicht zunehmend schlechter. Fehlgefaltete oder beschädigte Proteine sammeln sich an und stören die Zellfunktion. Dieser Prozess trägt wesentlich zur altersbedingten Abnahme der Zellqualität bei.
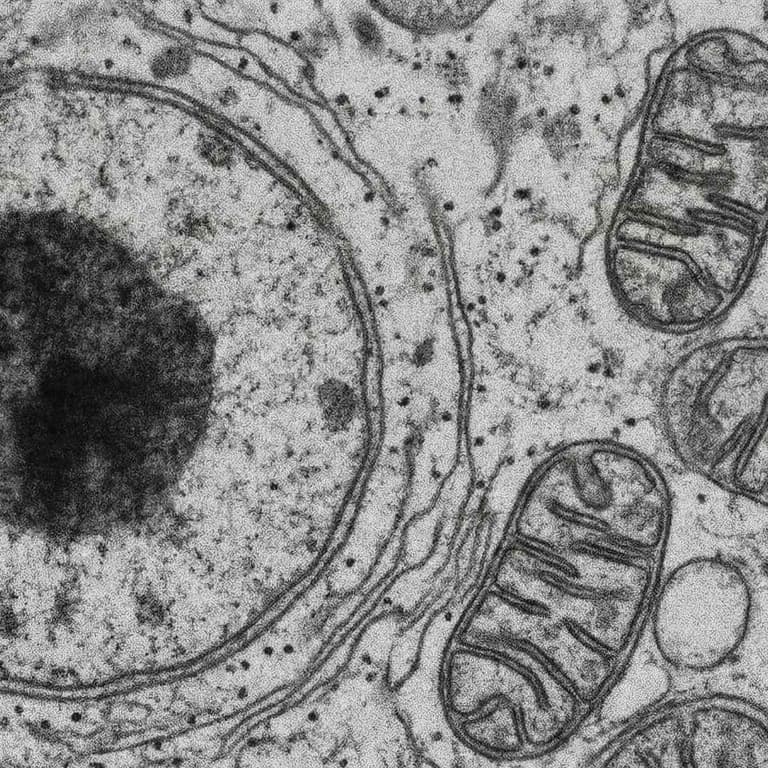
5. Gestörte Nährstoffsensorik
Der Körper nutzt spezielle Signalwege, um auf Nährstoffverfügbarkeit zu reagieren. Dazu zählen unter anderem Insulin-, mTOR- oder AMPK-Signalwege. Im Alter geraten diese Systeme aus dem Gleichgewicht, was Stoffwechselstörungen begünstigt. Die Folge sind reduzierte Reparaturprozesse und eine geringere Anpassungsfähigkeit an Belastungen.
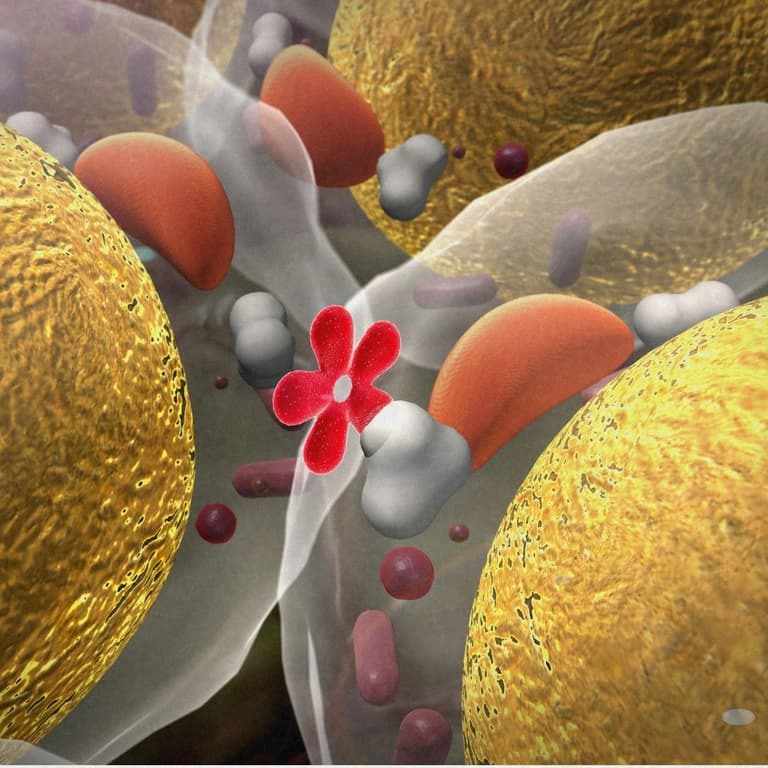
6. Mitochondriale Dysfunktion
Mitochondrien sind für die Energieversorgung der Zellen verantwortlich. Mit zunehmendem Alter sinkt ihre Effizienz, während gleichzeitig mehr reaktive Nebenprodukte entstehen. Das beeinträchtigt Energie, Ausdauer und Regeneration. Eine gestörte Mitochondrienfunktion gilt als zentraler Treiber vieler Alterungsprozesse.
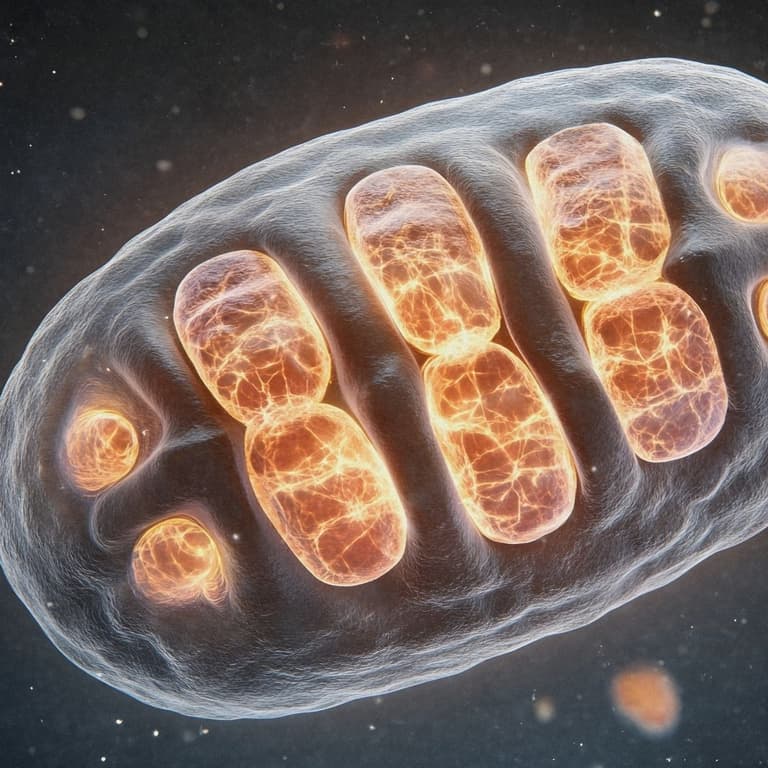
7. Zelluläre Seneszenz
Seneszente Zellen haben ihre Teilungsfähigkeit verloren, bleiben aber metabolisch aktiv. Sie setzen entzündliche Botenstoffe frei, die umliegendes Gewebe belasten können. Mit dem Alter nimmt ihre Zahl zu, während der Abbau dieser Zellen weniger effizient erfolgt. Dadurch verstärken sie systemische Entzündungsprozesse.
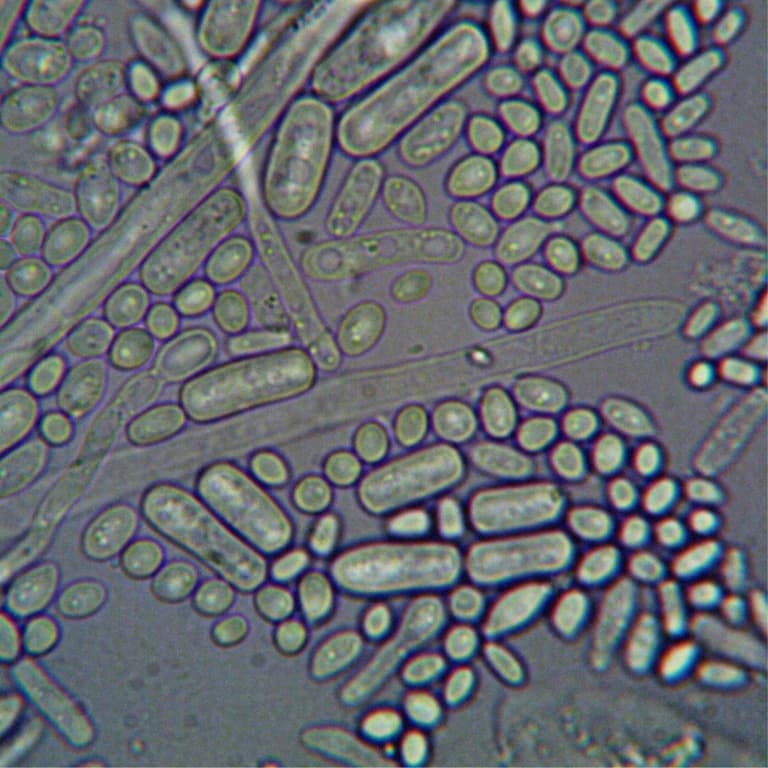
8. Stammzell-Erschöpfung
Stammzellen sind für die Erneuerung von Geweben verantwortlich. Im Alter sinkt sowohl ihre Anzahl als auch ihre Funktionsfähigkeit. Dadurch wird die Regeneration langsamer und weniger effektiv. Dieser Prozess erklärt, warum Heilung und Anpassung im höheren Alter mehr Zeit benötigen.
9. Veränderte Zell-zu-Zell-Kommunikation
Zellen stehen über Botenstoffe und Signale ständig miteinander in Austausch. Mit zunehmendem Alter verändern sich diese Kommunikationswege. Entzündliche Signale nehmen zu, während regulierende Mechanismen schwächer werden. Dies trägt zur systemischen Dysregulation des Körpers bei.
10. Chronische Entzündung („Inflammaging“)
Niedriggradige, dauerhafte Entzündungen sind ein eigenständiger Alterungstreiber. Sie entstehen durch ein Zusammenspiel aus Immunveränderungen, seneszenten Zellen und Stoffwechselprozessen. Inflammaging belastet Gewebe langfristig und steht im Zusammenhang mit vielen altersbedingten Erkrankungen. Es ist nicht nur Folge, sondern aktiver Motor des Alterns.
11. Dysbiose des Mikrobioms
Die Zusammensetzung der Darmmikrobiota verändert sich im Alter. Vielfalt und Stabilität nehmen ab, während entzündungsfördernde Bakterien zunehmen können. Diese Veränderungen beeinflussen Immunfunktion, Stoffwechsel und Entzündungsregulation. Das Mikrobiom gilt daher als wichtiger systemischer Faktor des Alterns.
12. Veränderungen der extrazellulären Matrix
Die extrazelluläre Matrix verleiht Geweben Struktur und Elastizität. Mit zunehmendem Alter verliert sie an Stabilität und Signalqualität. Das beeinflusst die Funktion von Zellen und Organen. Besonders Haut, Gefäße und Bindegewebe sind davon betroffen.
Warum die Hallmarks of Aging so relevant sind
Die 12 Hallmarks zeigen, dass Altern biologisch erklärbar und beeinflussbar ist. Sie machen sichtbar, wo Prozesse aus dem Gleichgewicht geraten – oft lange bevor Beschwerden entstehen. Genau hier setzt der moderne Longevity-Gedanke an.
Bei Healthii orientieren wir uns an diesen Mechanismen, um Produkte, Informationen und Empfehlungen biologisch sinnvoll, sicher und alltagstauglich einzuordnen. Ziel ist nicht, das Altern aufzuhalten, sondern gesunde Jahre aktiv zu unterstützen